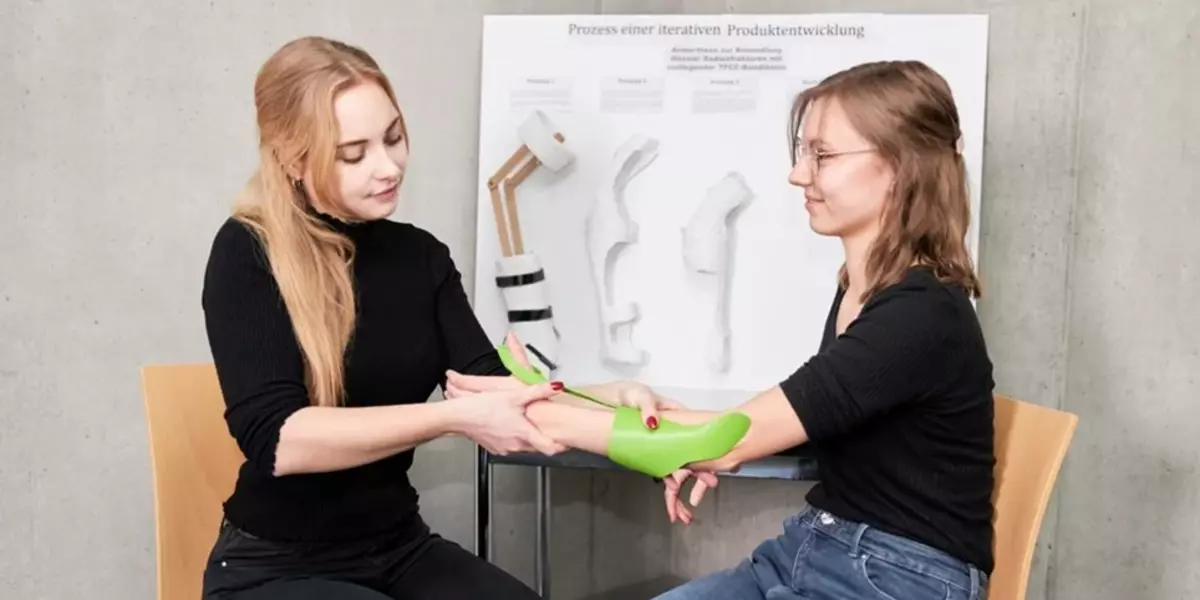
Was machen wir im Labor?
Die Entwicklung marktfähiger Medizinprodukte erfordert ein fundiertes Verständnis regulatorischer Rahmenbedingungen. Mit der europäischen Medizinprodukteverordnung (EU 2017/745, MDR) sind die Anforderungen an Hersteller deutlich gestiegen, während zugleich zahlreiche Auslegungs- und Umsetzungsfragen bestehen.
Das Labor Regulatory Affairs and Innovation for Medical Devices (RAI) befasst sich mit der praxisnahen Einordnung und Umsetzung regulatorischer Anforderungen aus ingenieurwissenschaftlicher Perspektive. Ziel ist es, Regulierung als gestaltbaren Rahmen für sichere, wirksame und innovative Medizinprodukte zu verstehen.
Unser Ansatz verbindet regulatorisches Denken mit Produktentwicklung, Innovationsmanagement und Anwenderperspektive. Das Labor bündelt Lehre, angewandte Forschung und Transfer und unterstützt Studierende, Start-ups und Industriepartner bei der Entwicklung und Markteinführung innovativer Medizinprodukte.
Das Labor ist Mitglied im Regensburg Center of Biomedical Engineering RCBE .
Lehre

Module Bachelor Biomedical Engineering:
- Regulatory Affairs
- Produktentwicklung in der Medizintechnik
- Biologische Sicherheit
- Diagnostische und Therapeutische Systeme
- Qualitätsmanagement in der Medizintechnik
Module Master Medizintechnik:
- Regelwerke für Medizinprodukte
- Innovationsmanagement
Forschung

Aktuelle Projekte im Labor RAI (Forschungsmaster):
- Patientenspezifische Inlays für Handgelenksorthesen
- Regulatorisch-ökonomische Erfolgsfaktoren für digitale Gesundheitsanwendungen
Unsere Kompetenzen
Laborausstattung
Stationäres und mobiles Equipment für Usability/Gebrauchstauglichkeitstests von Medizinprodukten und DiGA.
Team
Standort
Regulatory Affairs and Innovation for Medical Devices Lab
Galgenbergstr. 30
93053 Regensburg
Raum: A 202
Tel: +49 (0)941 943-5298